Neue Immuntherapie bei Schimmelpilzinfektion
11.10.2022Die Ergebnisse einer aktuellen Studie des Uniklinikums Würzburg geben Hoffnung auf neu entwickelte, alternative Therapieoptionen bei Pilzinfektionen.
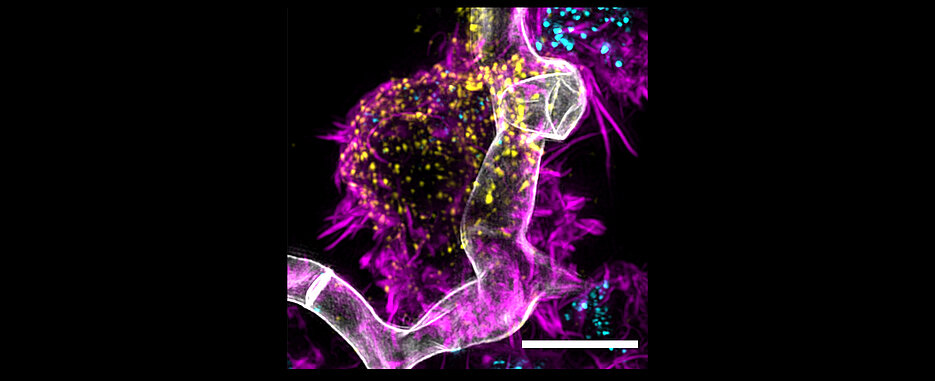
Wir atmen nahezu täglich und überall auf der Welt die Sporen des Aspergillus fumigatus ein. Der Schimmelpilz ist bei einer guten Immunabwehr relativ harmlos. Bei Menschen, deren Immunsystem stark geschwächt ist, zum Beispiel nach Chemotherapien oder Knochenmarktransplantationen, kann der Aspergillus fumigatus jedoch schwere, oft tödlich verlaufende Infektionen verursachen. Auch in Verbindung mit einer Covid-Infektion oder Grippe kann der Aspergillus fumigatus die Lungenfunktion beeinträchtigen.
Doppelt wirksam: Af-CAR-T-Zellen wirken gegen Pilz und aktivieren weitere Immunzellen
Am Uniklinikum Würzburg haben Forscherinnen und Forscher aus der Medizinischen Klinik II erstmals bestimmte Immunzellen, so genannte T-Zellen, gentechnisch verändert, wodurch die körpereigene Immunabwehr gegen diese Art von Schimmelpilzen besser aktiviert und effektiver geschützt wird. Die umprogrammierten T-Zellen tragen auf ihrer Oberfläche „chimäre Antigenrezeptoren“, kurz CAR. Mit diesen Biosensoren können die T-Zellen die spezifische Struktur des Schimmelpilzes wesentlich besser erkennen und durch die Freisetzung bestimmter körpereigener Botenstoffe zerstören.
Die T-Zellen mit den Aspergillus fumigatus-spezifischen CARs (Af-CARs) wirken aber nicht nur direkt gegen den Pilz, sondern auch indirekt: „In unseren präklinischen Labormodellen haben wir beobachtet, dass die Af-CAR-T-Zellen in der Lage sind an den Ort der Pilzinfektion zu gelangen, und die Rekrutierung und Aktivierung zusätzlicher Zellen des körpereigenen Immunsystems zu kontrollieren. Insbesondere, die Af-CAR-T-Zellen aktivieren Makrophagen und verstärken somit die Wirkung des Immunsystems gegen den Schimmelpilz“, erklärt Dr. Michelle Seif, Postdoc in der AG Löffler und AG Hudecek und Erstautorin der Studie, die jetzt im Journal Science Translational Medicine veröffentlicht wurde.
Studie legt Grundlagen für neue immuntherapeutische Methoden
„Unsere Studie veranschaulicht das große Potenzial gentechnisch veränderter T-Zellen zur Behandlung aggressiver Infektionskrankheiten, die mit herkömmlichen antimikrobiellen Therapien nur schwer in den Griff zu bekommen sind. Sie bildet die Basis für eine zukünftige T-Zelltherapie zur Behandlung von Pilzinfektionen und vielen weiteren Infektionserkrankungen“, resümiert Professor Dr. Jürgen Löffler, Leiter der AG Löffler, die am Uniklinikum Würzburg die Aspergillose, wie die Schimmelpilzinfektion in der Fachsprache heißt, erforscht.
Die Entwicklung und klinische Umsetzung der CAR-T-Zelltherapien bei Tumorerkrankungen ist seit vielen Jahren ein herausragender Schwerpunkt am Uniklinikum Würzburg. Die Immunzellen der Patientinnen und Patienten werden umprogrammiert, um sie gezielt zur Zerstörung von Krebszellen auszustatten. Der chimäre Antigenrezeptor hilft den T-Zellen die Krebszellen zu erkennen und zu eliminieren. „Mit den präklinischen Untersuchungen zur gentechnisch hergestellten Immunzelltherapien bei Schimmelpilzinfektionen bringen wir in gewisser Weise das Thema dorthin zurück, wo es entstanden ist“, bemerkt Professor Dr. Michael Hudecek, der gemeinsam mit Jürgen Löffler Letztautor der Studie ist.
Die adaptive Immuntherapie mit T-Zellen begann im Bereich der Infektionskrankheiten durch das Cytomegalievirus, das zur Familie der Herpesviren gehört. Professor Herrmann Einsele, Direktor der Medizinischen Klinik II am UKW, hat bereits in den 1990er Jahren als erster Mediziner in Europa Patientinnen und Patienten mit Cytomegalievirus-spezifischen T-Zellen behandelt. „Unsere Motivation war es, die CAR-T-Zelltherapie als ein in der Medizin universell anwendbares Therapieprinzip zu demonstrieren“, so Hudecek.
Vorbereitung für Einsatz von klinischen Studien
Die Ergebnisse der Studie ermutigt das Würzburger Team, die Af-CAR-T-Zelltherapie zur Behandlung von Infektionen durch Aspergillus fumigatus in ersten klinischen Studien umzusetzen und zu evaluieren. „Derzeit erarbeiten wir weitere Konzepte, um das Aspergillus-CAR-T-Zell-Produkt skalierbar zu machen und für den klinischen Einsatz vorzubereiten“, verlautbart Jürgen Löffler. „Wir hoffen, dass durch diese zukünftige, stark translationale Ausrichtung des Projekts in der Zukunft möglichst viele Patientinnen und Patienten von der neuartigen Technologie profitieren können.“
Publikation
Die Studie “CAR T cells targeting Aspergillus fumigatus are effective at treating invasive pulmonary aspergillosis in preclinical models” wurde publiziert im Journal Science Translational Medicine DOI: 10.1126/scitranslmed.abh1209.
Partnerinnen und Partner
Kooperiert hat das Würzburger Team mit Professor Dr. Frank Ebel von der Ludwig-Maximilians-Universität München, Professorin Dr. Luigina Romani von der Universität Perugia, Professor Emmanuel Donnadieu von der Université de Paris, Dr. Kerstin Hünniger vom Leibniz Institut für Naturforschung und Infektionsbiologie in Jena und Dr. Lewis White von Public Health Wales in Cardiff und deren jeweiligen Teams.
Förderungen
Gefördert wurden die Untersuchungen vom Bundesministerium für Bildung und Forschung (Projekt ART4Fun), von der Wilhelm Sander Stiftung (Projekt 2020-017-1), von der Deutschen Forschungsgemeinschaft im Rahmen der Sonderforschungsbereiche TransRegio 124 „FungiNet“ und TransRegio 221 „GvL/GvH“, vom LMU Medical School-Fellowship im Rahmen des Förderprogramms für Forschung und Lehre, von der European Union (Horizon 2020 & EFRE-programme) und von der Innovative Medicine Initiative 2 Joint Undertaking (T2EVOLVE).